卫生署今日(七月六日)指令两间持牌药物批发商阿特维斯(香港)有限公司(阿特维斯)及港联医药供应有限公司(港联),从市面回收五款含有缬沙坦的药剂制品,作为预防措施,因为相关原料被发现含有杂质。
受影响产品如下:
产品 香港注册编号 注册证书持有人
Valtensin 160毫克药片 HK-61786 阿特维斯
Valtensin 80毫克药片 HK-61787 阿特维斯
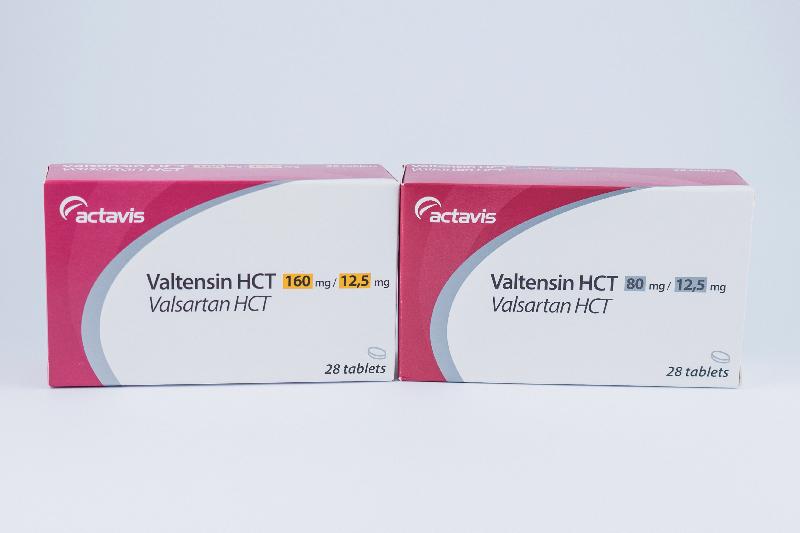
Valtensin HCT 药片160/12.5毫克 HK-61784 阿特维斯
Valtensin HCT 药片80/12.5毫克 HK-61785 阿特维斯
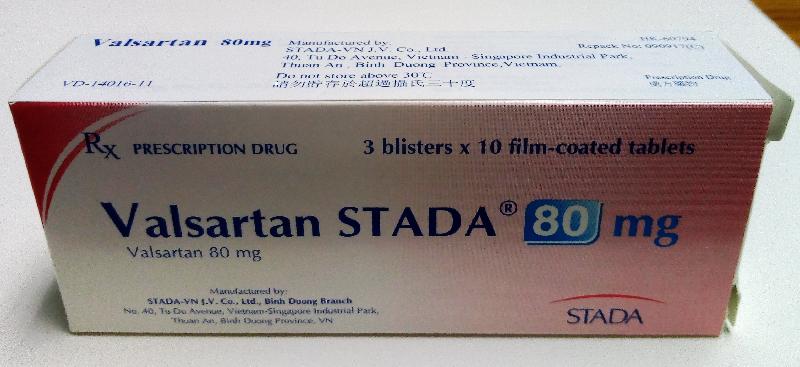
Valsartan Stada 80毫克药片 HK-60794 港联
卫生署透过其监察系统,得悉一所内地制造商生产的缬沙坦原料被发现含有杂质N-亚硝基二甲胺(NDMA),有关原料为一些药剂制品的主要成分。该杂质基于实验室测试被列为可能令人类患癌的物质。
至今,上述在港注册的产品经批发商确定含有受影响的原料。卫生署的调查仍在进行。
根据该内地制造商的初步调查显示,NDMA存于缬沙坦原料中相信与其生产方法有关。
含有缬沙坦的产品属处方药物,用于治疗高血压及心脏衰竭,分别有单一成分产品及结合其他主要成分的产品。
根据阿特维斯及港联的资料,上述产品已供应予本地私家医生及药房。其中Valtensin 80毫克及160毫克药片亦有供应予医院管理局。
两间药物批发商均已设立热线(阿特维斯:3188 4288;港联:2806 3112)回答相关查询。
卫生署至今未有接获任何涉及上述受影响产品的不良反应报告。
正在服用上述产品的病人不应自行停止服用药物,他们应向其医护人员谘询意见,以作适当安排。
转载自香港特区政府网页∶
http://sc.isd.gov.hk/TuniS/www.info.gov.hk/gia/general/201807/06/P2018070600859.htm