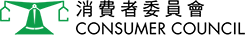卫生署今日(十二月十日)同意持牌药物批发商美国礼来亚洲公司(礼来)从批发商回收一个批次(批次编号:D086749A)的力挽生浓缩静脉注射液100毫克/10毫升(香港注册号码:HK-64421)(力挽生),因为产品有潜在品质问题。
卫生署接获礼来通知,指一批上述产品中发现混有一支培养液。这批次产品经包装后以批次编号D086749A供应予香港。生产商的初步调查指该支培养液可能从较早前的工序中遗留并混入有关力挽生批次。这支培养液并不含有主要成分,而其内含物的颜色与含量均与力挽生不同;因此,培养液是可以透过目测分辨出来。作为预防措施,礼来决定从批发层面回收上述批次产品。
上述产品含有雷莫芦单抗,是用于治疗晚期胃癌、扩散性大肠直肠癌及非小细胞肺癌的处方药物。根据礼来的资料,受影响批次产品曾供应给医院管理局、私家医院及私家医生。
礼来已设立热线(2964 2966)回答相关查询。
医护人员在使用上述产品前应先仔细检视注射瓶并留意内含物的顔色。培养液瓶内含量较力挽生的含量少,其内含物呈黄至浅啡色。礼来将会为受影响的医生及医院提供指引,并于其他不受影响批次供港时替换受影响批次的产品。
卫生署至今未有接获涉及受影响批次产品的不良反应报告。卫生署会密切监察有关回收。
曾使用上述产品的病人如有疑问,应向其医护人员谘询意见。
转载自香港特区政府网页︰
https://www.drugoffice.gov.hk/gb/unigb/www.drugoffice.gov.hk/eps/news/showNews/Batch+Recall+of+Cyramza+Concentrate+For+Solution+For+Infusion+100mg%EF%BC%8F10ml+%28with+photo%29/pharmaceutical_trade/2019-12-10/tc/38957.html