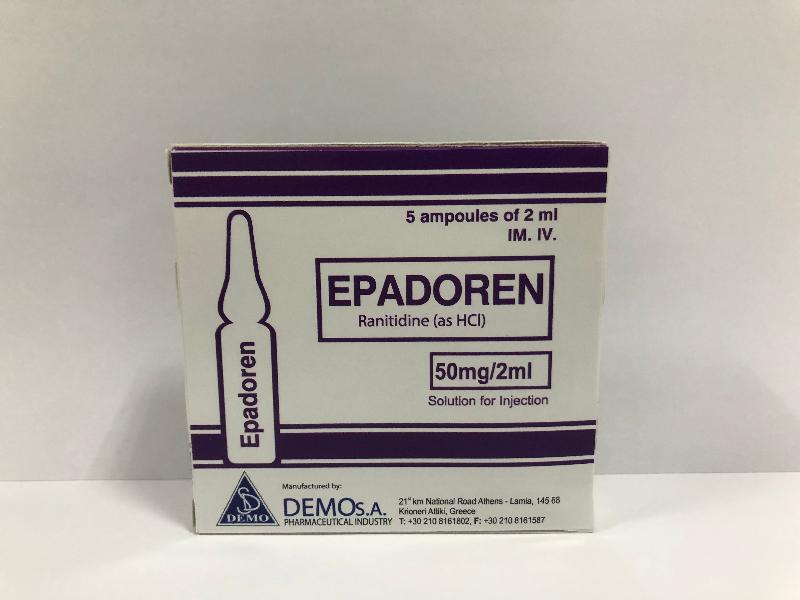
卫生署今日(十月十一日)同意持牌药物批发商显荣行有限公司(显荣行)采取预防措施,从市面回收一款含有雷尼替丁的产品,即Epadoren 50毫克/2毫升注射液(香港注册编号:HK-61752),因为相关产品可能含有杂质。
卫生署今日接获显荣行通知,指有关产品的制造商基于近期就有关杂质的外地报道,故怀疑上述产品可能含有杂质N-亚硝基二甲胺(NDMA)。基于实验室测试,NDMA被列为可能令人类患癌的物质。作为预防措施,显荣行自愿从市面回收受影响的产品。
卫生署得悉一些含有雷尼替丁的产品在外国被发现含有NDMA,并自九月二十四日起先后共批准了七款含有雷尼替丁产品的自愿回收。卫生署正继续从市面上抽取含有雷尼替丁产品样本作检验。卫生署亦得悉海外药物监管机构正评估含有雷尼替丁产品被发现含杂质对安全性的影响。署方会密切监察事件的发展和海外药物监管局就该药物发出更新的安全评估,以考虑任何必要的跟进行动。卫生署亦已于九月十八日发信予医护人员,通知他们有关事件。
上述产品是用于治疗胃部疾病的处方药物。根据显荣行的资料,受影响产品曾供应予私家医院、本地医生、兽医和药房。
显荣行已设立热线电话(2541 5731)解答相关查询。
卫生署发言人说:「卫生署至今未有接获涉及有关产品的不良反应报告,并会密切监察有关回收。」
须使用上述产品的病人应向其医护人员谘询意见,以作适当安排。市面上有其他替代药物可作相类用途。
转载自香港特区政府网页∶
https://sc.isd.gov.hk/TuniS/www.info.gov.hk/gia/general/201910/11/P2019101100639.htm